Deshalb sollten auch bei klinischem Verdacht auf eine spezielle AAV immer:
- c- und pANCA und
- PR3- und MPO-Ak angefordert werden!
Savige J, Gillis D, Benson E et al. (1999) International consensus statement on testing and reporting of Antineutrophil Cytoplasmic Antibodies (ANCA). Am J Clin Pathol 111:507–513. doi: 10.1093/ajcp/111.4.507
Savige J, Dimech W, Fritzler M et al. (2003) Addendum to the International Consensus Statement on testing and reporting of antineutrophil cytoplasmic antibodies. Quality control guidelines, comments, and recommendations for testing in other autoimmune diseases. Am J Clin Pathol 120:312–318. doi: 10.1309/WAEP-ADW0-K4LP-UHFN
Schirmer, J.H., Aries, P.M., de Groot, K. et al. S1-Leitlinie Diagnostik und Therapie der ANCA-assoziierten Vaskulitiden. Z Rheumatol 76 (Suppl 3), 77–104 (2017). doi.org/10.1007/s00393-017-0394-1
Bossuyt, X., Cohen Tervaert, JW., Arimura, Y. et al. Revised 2017 international consensus on testing of ANCAs in granulomatosis with polyangiitis and microscopic polyangiitis. Nat Rev Rheumatol 13, 683–692 (2017). doi.org/10.1038/nrrheum.2017.140
Damoiseaux J, Csernok E, Rasmussen N, et al. Detection of antineutrophil cytoplasmic antibodies (ANCAs): a multicentre European Vasculitis Study Group (EUVAS) evaluation of the value of indirect immunofluorescence (IIF) versus antigen-specific immunoassays Annals of the Rheumatic Diseases 2017;76:647-653. doi.org/10.1136/annrheumdis-2016-209507
Seit 2017 gibt es eine erste deutsche S1-Leitlinie zur ANCA-assoziierten Vaskulitis. Dennoch hat sich die Diagnostik-Empfehlung bislang nicht flächendeckend durchgesetzt. Sehr häufig entspricht das Anforderungsprofil den Empfehlungen verschiedener internationaler Konsensus. Dabei sprechen klare medizinische Gründe für die nationale Leitlinie!
Zu den ANCA-assoziierten Vaskulitiden (AAV) gehören die
AAV gehören mit einer Prävalenz von 150/1 Million zu den seltenen Erkrankungen. Dennoch erfordern sie eine besondere Aufmerksamkeit, da sie zu einem der wenigen diagnostischen Notfälle in der Autoimmunologie werden können. Wie die meisten anderen Autoimmunerkrankungen nehmen zwar auch die AAV oft einen jahrelangen chronischen Verlauf. Die anfängliche Symptomatik wird wegen der Differenzialdiagnosen mit sehr viel höheren Prävalenzen jedoch oft nicht als Beginn einer AAV erkannt.
Treten die ersten spezifischen Symptome auf, ist das Zeitfenster bis zum Organversagen oft nur kurz (siehe Fallbeispiel unten).
Umso wichtiger ist dann eine schnelle und sensitive Diagnostik!
Abb. 1 Eigenes Fallbeispiel mit typischem Symptomverlauf (vgl. mit „Klassische Symptome der GPA“ rechts)
Erstmals an eine AAV gedacht wurde mit Auftreten der Hämoptoe. Bei telefonischer Befundübermittlung des positiven cANCA/PR3-Ak begannen bereits weitere Organe zu versagen. Der Patient überlebte nach einwöchiger Intensiv-Therapie mit künstlichem Koma.
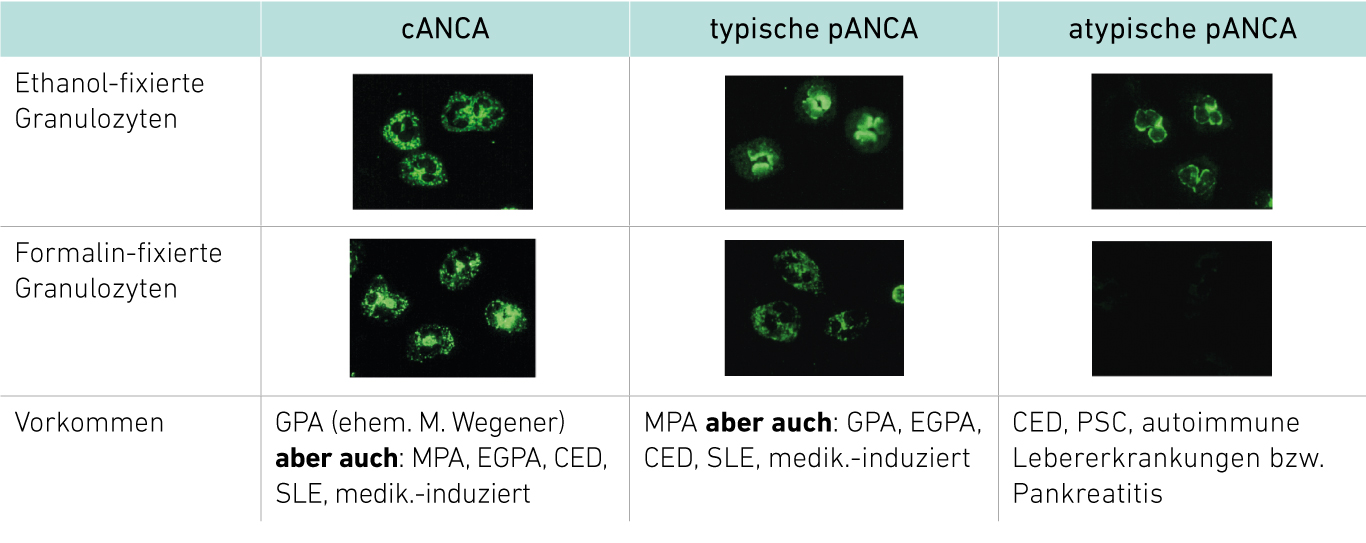

Abb. 2. ANCA-Diagnostik Immunfluoreszenztest (IFT)
Positive Befunde auf Ethanol-fixierte Granulozyten müssen auf Formalinfixierte Granulozyten weiter differenziert werden. Die für eine AAV diagnostisch relevanten ANCA bestätigen sich hier typischerweise mit einer zytoplasmatischen Fluoreszenz, während die sogenannten atypischen pANCA (eher hinweisend auf autoimmune Leber- oder chronisch entzündliche Darmerkrankungen) für gewöhnlich negativ ausfallen.
CED: Chronisch-entzündliche Darmerkrankung, SLE: systemischer Lupus erythematodes, PSC: primär sklerosierende Cholangitis
Bei einer GPA (ehemals M.Wegener) werden zwar vornehmlich cANCA mit Spezifität PR3-Ak beobachtet, jedoch können auch pANCA oder MPO-Ak nachgewiesen werden. Ebenso wird bei der Mikroskopischen Polyangiitis zwar meistens die Kombination pANCA und MPO-Ak gefunden, jedoch immer wieder auch cANCA oder PR3-Ak (siehe Tab. 1).
Tab. 1 Antikörperverteilung bei den verschiedenen Formen der AAV
| cANCA (%) | PR3-Ak (%) | pANCA (%) | MPO-Ak (%) | |
|---|---|---|---|---|
GPA | 50–90 | 69–90 | 5–25 | 8–12 |
MPA | 5–30 | 3–6 | 40–89 | 48–86 |
EGPA | 10–20 | 9 | 20–70 | 69 |
Die Zahlen belegen eindrücklich die Notwendigkeit, bei Verdacht auf eine AAV, unabhängig von der Form, grundsätzlich beide ANCA-Spezifitäten bzw. beide EIA anzufordern, da es in nicht unerheblichem Maße diagnostische Überschneidungen gibt. Sie zeigen ebenfalls die mittlerweile vergleichbar guten Sensitivitäten von ANCA- und EIA-Testung. Nicht darstellbar in dieser weitverbreiteten Tabellenform ist die Erfassung unterschiedlicher Patientengruppen durch EIA und IFT, so dass trotz vergleichbarer Gesamt-Sensitivität die Wichtigkeit der parallelen Anforderung von EIA und IFT regelhaft unterschätzt wird.
Bis 2017 galt eine internationale KonsensusEmpfehlung aus 1999 (1), die 2003 (2) bestätigt wurde. Damals waren die EIA-Teste dem IFT in Sensitivität und Spezifität noch deutlich unterlegen, weshalb folgerichtig primär die Untersuchung der ANCA im IFT empfohlen wurde. Lediglich positive ANCA-Ergebnisse wurden mittels Testung auf PR3- und MPO-Ak im EIA weiter differenziert. Mit der Weiterentwicklung der EIA-Teste kann diese Empfehlung für die AAV als überholt gelten. Möglicherweise verwirrend ist, dass für die ANCA-Diagnostik im Rahmen von chronisch entzündlichen Darmerkrankungen bzw. autoimmunen Leber- oder Pankreas-Erkrankungen unverändert die primäre Untersuchung der ANCA im IFT gilt.
Die deutsche S1-Leitlinie aus 2017 (3) empfiehlt hingegen die parallele Testung der ANCA im IFT und der MPO-/ PR3-Ak im EIA. Ziel der Empfehlung ist die schnelle und bestmögliche Diagnostik. Zwar weisen die neuesten Testgenerationen von EIA und IFT vergleichbare Sensitivitäten und Spezifitäten auf, jedoch erkennen EIA und IFT in bis zu 10% andere Patienten. Nur durch die parallele Untersuchung der beiden Testsysteme kann die derzeit maximal mögliche Sensitivität erreicht werden. Der Wegfall der Stufendiagnostik erspart zudem Zeit – ein wichtiger Faktor, wenn der Verdacht erst spät im Verlauf aufkommt und nur durch einen schnellen Therapiebeginn ein Multiorganversagen noch zu verhindern ist
Etwas später im Jahr 2017 wurde ein neuer internationaler Konsensus (4) veröffentlicht, der die ausschließliche Testung von MPO-/PR3-Ak im EIA empfiehlt. Eine Indikation für die ANCA-Testung im IFT wird nur noch in Ausnahmefällen gesehen. Die Zielsetzung hier ist eher technischer Natur – es geht um eine bessere Vergleichbarkeit der Testsysteme. Die Empfehlung basiert auf den Ergebnissen der internationalen EUVAS-Studie (5), die eine gute Vergleichbarkeit für EIA-Teste untereinander, nicht aber für IFTs untereinander zeigte. Allerdings wurden nur zwei IFTs miteinander verglichen, von denen einer nicht nach Standardbedingungen abgearbeitet wurde. Die Gesamt-Sensitivität bleibt bei diesem Regime unverändert, da hier lediglich die diagnostische Lücke der IFTs gegen die der EIAs getauscht wird.
| EBM | GOÄ | |||
|---|---|---|---|---|
| Ziffern | € | Ziffern | € (1,15-fach) | |
| ANCA (IFT)* | 32496 | 10,10 € | 3826H2 | 19,44 € |
| bei Titerbestimmungen im positiven Fall: 3853 | 34,19 € | |||
| PR3-Ak (EIA) | 32496 | 10,10 € | 3874 | 30,16 € |
| MPO-Ak (EIA) | 32496 | 10,10 € | 3873 | 30,16 € |
Abrechnung
*Die EBM-Ziffer für den ANCA-IFT wird nur einmalig berechnet, unabhängig davon, ob isoliert ein p- bzw. c-ANCA oder aber beide Parameter gemeinsam angefordert wurden. Da es sich bei pANCA mit perinukleärer Fluoreszenz bzw. bei cANCA mit cytoplasmatischer Fluoreszenz lediglich um eine Beschreibung des Fluoreszenzmusters innerhalb der Granulozyten handelt, sind sie in einem gemeinsamen Untersuchungsgang zu beurteilen und folglich nur einmal abzurechnen. Durch die gemeinsame Anforderung von p- und c-ANCA entstehen folglich keine zusätzlichen Kosten!
Anders als im EBM gibt es bei der GOÄ-Bereich zwei Abrechnungsziffern, wenn im positiven Fall zur Titerbestimmung weitere Verdünnungsansätze durchgeführt werden müssen. Die erforderlichen Mehrfach-Bestimmungen werden etwas höher vergütet.